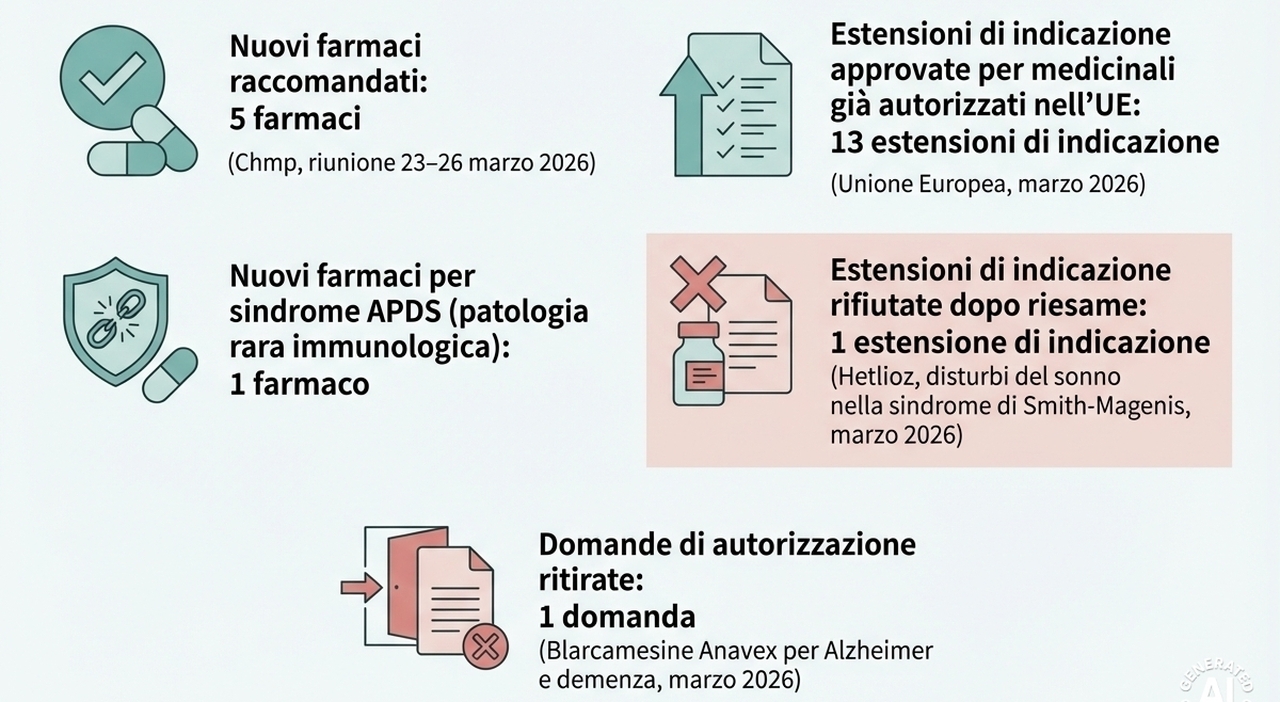
Il Comitato per i medicinali per uso umano (Chmp) dell’Agenzia europea per i medicinali (Ema) ha raccomandato l’approvazione di cinque nuovi farmaci, destinati in particolare al trattamento di due forme di tumore difficili da trattare - il carcinoma della vescica non responsivo alle terapie standard e il tumore al polmone a piccole cellule in fase avanzata - oltre che di una rara malattia immunologica ereditaria, la sindrome APDS, potenzialmente letale e priva di opzioni terapeutiche mirate fino a tempi recenti. Le decisioni sono arrivate al termine della riunione tenutasi dal 23 al 26 marzo 2026.
Tra le novità più rilevanti spicca Adstiladrin (nadofaragene firadenovec), per il quale è stata raccomandata un’autorizzazione condizionata. Il farmaco è destinato ai pazienti adulti affetti da carcinoma vescicale non muscolo-invasivo non responsivo al trattamento con Bacillus Calmette-Guérin (BCG), offrendo una nuova opzione terapeutica in un contesto clinico complesso.
Sempre in ambito oncologico, il Chmp ha espresso parere favorevole per Imdylltra (tarlatamab), indicato per il trattamento del tumore al polmone a piccole cellule in fase estesa recidivata, una forma particolarmente aggressiva e con limitate possibilità di cura. A questo si aggiunge il via libera a Zepzelca (lurbinectedin) come terapia di mantenimento per pazienti con la stessa patologia che non hanno mostrato progressione dopo il trattamento iniziale.