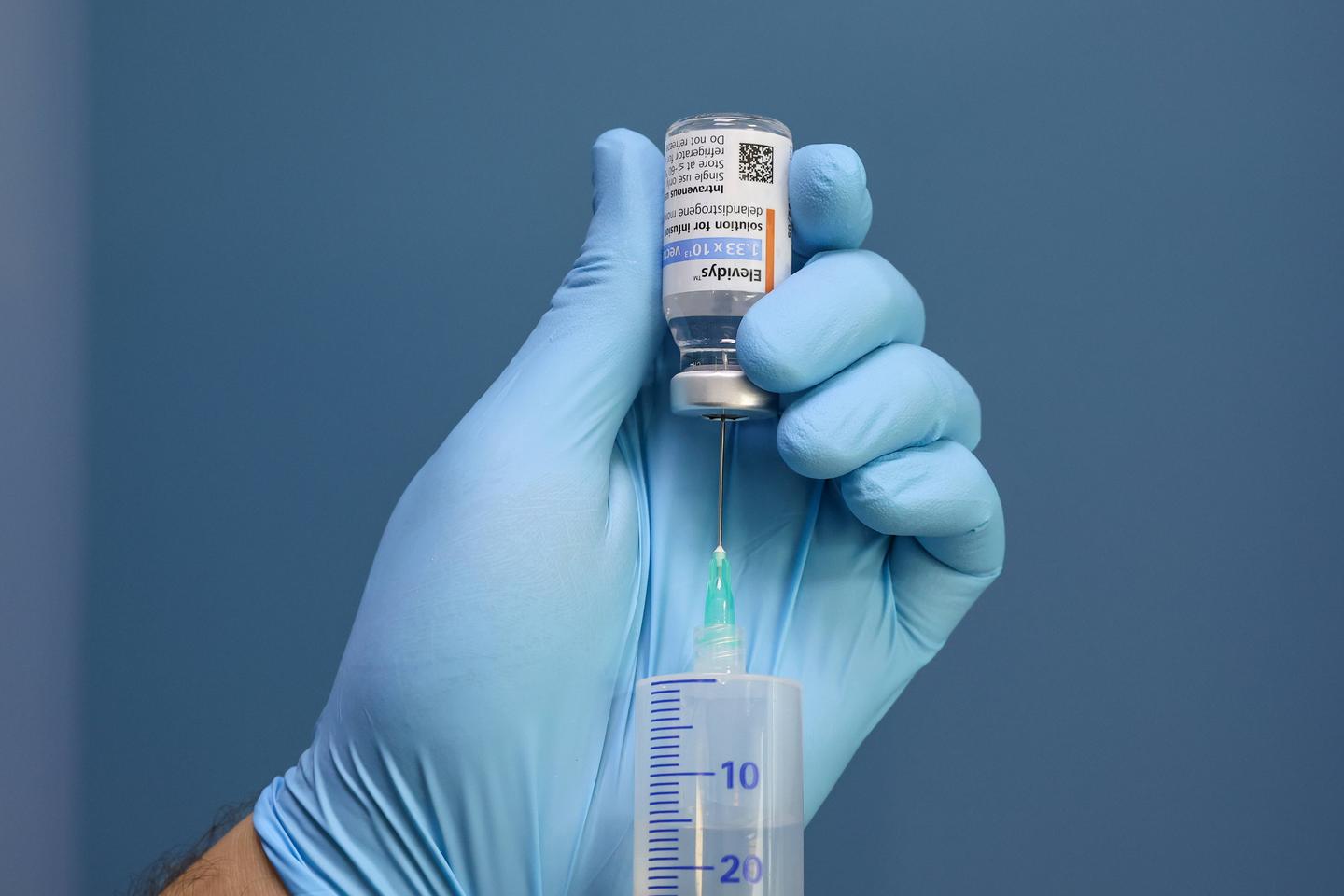
(ANSA-AFP) - ROMA, 15 NOV - La Food and Drug Administration (FDA) statunitense ha annunciato venerdì di voler limitare l'accesso a un trattamento innovativo per la distrofia muscolare di Duchenne, una rara e grave malattia genetica, e di aver emesso un avviso formale in seguito alla morte di due adolescenti.
Elevidys, terapia genica sviluppata dall'azienda americana Sarepta Therapeutics, è stata approvata negli Stati Uniti per i bambini dai quattro anni in su affetti da questa patologia che causa la degenerazione progressiva dei muscoli.
Colpisce principalmente i giovani, con un'aspettativa di vita media dei pazienti di 28 anni.
Il trattamento di Sarepta Therapeutics, che appartiene a una nuova classe di terapie innovative, aveva suscitato grandi speranze.
Tuttavia, i dati deludenti sull'efficacia e i recenti decessi hanno alimentato le critiche al trattamento.