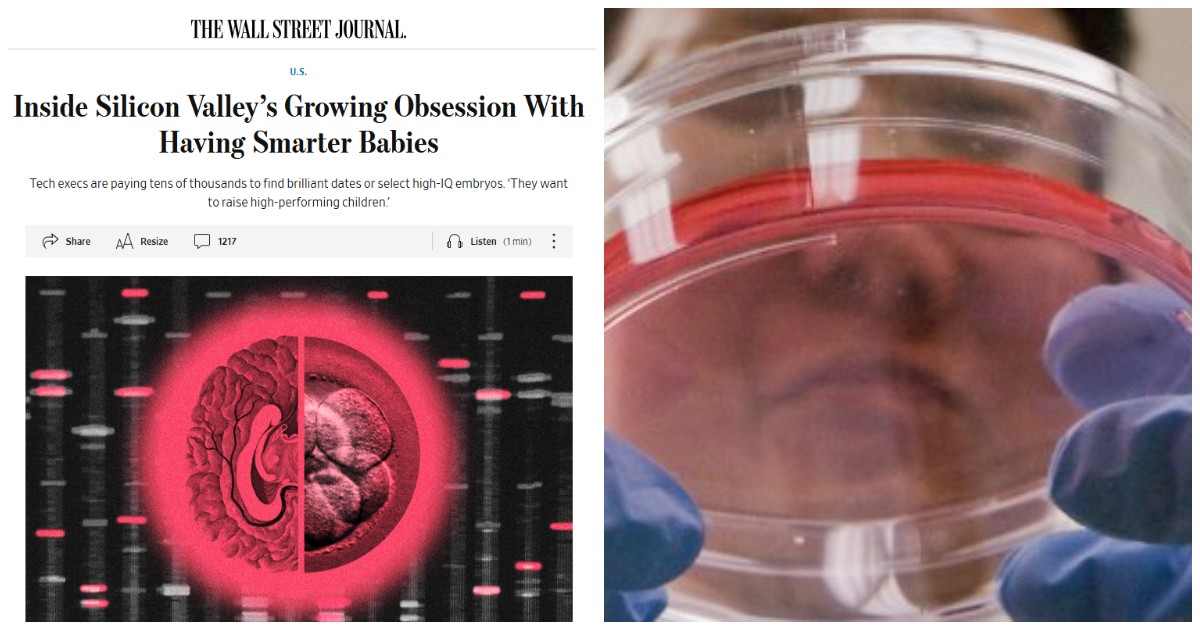
L’obiettivo dichiarato – anzi, sarebbe più corretto dire trapelato, visto che esiste un patto di massima segretezza tra gli attori della vicenda – è far nascere bambini sani, geneticamente modificati in modo da evitare malattie genetiche ereditarie. O malattie ossee o cardiache o rischi cardiovascolari e chissà che altro. Ma c’è chi già pensa che le modifiche genetiche rese possibili dalla tecnica Crispr, anche nota come il taglia e cuci del DNA – una forbice molecolare in grado, quindi, di sostituire con altri sani i geni responsabili di malattia – possano consentire di individuare gli embrioni che potenzialmente possono avere un quoziente intellettivo maggiore.
Avvenire: si gioca a fare Dio
O, perché no, magari dar vita a individui più alti e performanti, magari con tendenza al normopeso o di altezza superiore alla media. Perché dal desiderare un bambino sano al pensiero di averne uno perfetto il passo è breve, e il desiderio inconfessabile. Insomma, come titolava il quotidiano cattolico Avvenire, si tenta di creare in provetta il bambino perfetto, per fare a gara con Dio.
La moratoria su manipolazione embrioni
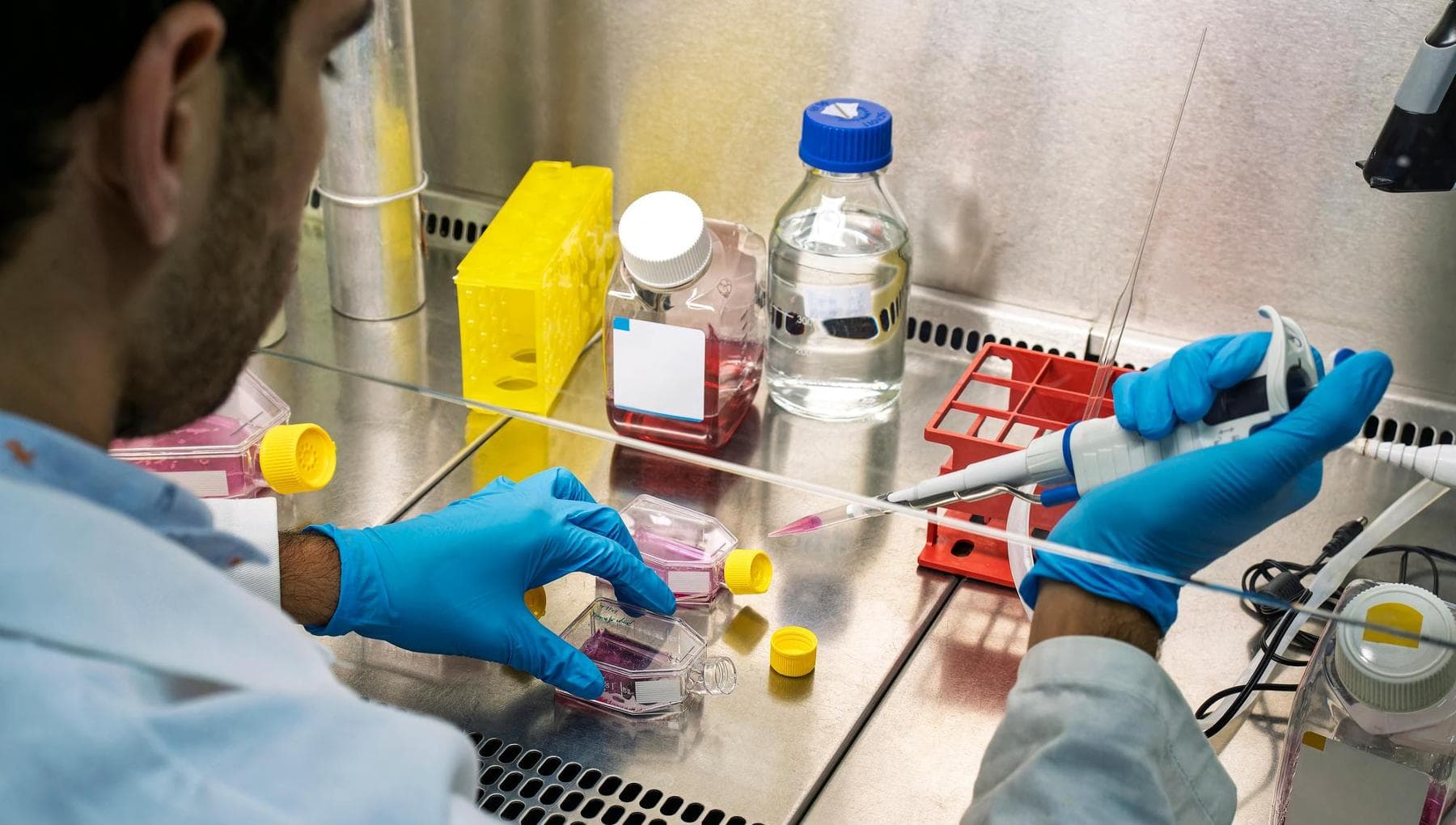
Ma al di là delle imprescindibili questioni etiche – che non a caso hanno imposto una moratoria in quasi tutto il mondo all’utilizzo della tecnica Crispr nelle cellule riproduttive e negli embrioni – che cosa c’è di fattibile in Preventive, start-up della Silicon Valley fondata dal genetista Lucas Harrington e finanziata con oltre 30 milioni di dollari da alcuni tra i maggiori imprenditori tecnologici americani, come Sam Altman di OpenAI e Brian Armstrong, guru delle criptovalute con Coinbase? E qual è il sogno che davvero inseguono? Davvero quello di un bambino senza malattie genetiche o con minori rischi cardiovascolari, come dichiarano, o piuttosto quello di un essere del quale si possono scegliere preventivamente caratteristiche fisiche o addirittura attitudini? E il termine eugenetica, utilizzato da alcuni per contestare la tecnica, è davvero così fuori luogo? Inoltre, a chi sarebbe davvero accessibile una tecnologia di questo tipo, visto che il trattamento per l’editing genetico dell’anemia falciforme approvato da Fda costa più di 2.2 milioni di dollari? Tante domande, e la prima è se è un’idea delirante, come sostiene Fyodor Urnov, direttore dell’Innovative Genomics Institute dell’Università della California-Berkeley.